74 sidor med rekommendationer kring vasopressorer, eFAST, blodprodukter, mm vid trauma!
Pupillreflex på igenmurat öga?
Indirekt ljusreflex innebär att du lyser i ett öga och letar efter pupillsammandragning i det andra. Om en patient har en skada i ett öga, eller om det inte går att öppna ögat på grund av ett hematom, kan den indirekta ljusreflexen utnyttjas. En linjär ultraljudsprob placeras transversellt över det skadade ögat (skydda ögat med en Tegaderm och applicera gel utanpå). Lys sedan i det friska ögat och leta efter pupillsammandragning på ultraljudet. Här är en tutorial från 5minSono:
Föreläsningar om POCUS vid trauma
Bjarni Árnason arbetar på PMI, Karolinska, Solna. Här föreläser han om point of care ultrasound (POCUS) under kursen i traumAAnestesi 2016:
Efter Bjarni talade jag mer om POCUS vid trauma (och sen hade deltagarna POCUS workshop):
Fokuserat TEE vid trauma -när, var, hur?
I ett tidigare inlägg berättade jag om hur TEE var till stor hjälp vid handläggningen av ett traumafall. På Karolinskas ultraljudskurs för två veckor sedan föreläste Johan Nordström om en förenklad TEE-algoritm som han använder vid hjärtstopp, svåra traumafall och andra fall av odifferentierad shock.
När en patient kommer in på traumarummet i shock så bör man utesluta att det beror på ventilpneumothorax eller tamponad och därefter göra antagandet att det beror på blödning någonstans. I vissa fall fortsätter patienten att vara cirkulatoriskt instabil trots att man har tagot höjd för ovanstående och då kan TEE vara till stor hjälp att diffa mellan fortsatt hypovolemi, missad eller progredierande tamponad, neurogen hjärtsvikt efter TBI, hjärtkontusion, klaffruptur pga waterhammer effect, pumpsvikt (pga reperfusion injury??) efter period med extrem hypovolemi.
Länk till Johan Nordströms TEE-föreläsning
Länk till The American Association for the Surgery of Trauma: Blunt Cardiac injury
Vad har POCUS för roll i traumaomhändertagandet?

På traumAAnestesi-kursen som drar igång på måndag kommer Bjarni Árnason att föreläsa om varför vi anser att ultraljud har en plats i det prehospitala omhändertagandet, på traumarummet, i operationssalen och på IVA.
Här är en länk till hans föreläsning samt några länkar, artiklar och podcasts som han rekommenderar inför sin föreläsning:
Sonospot: Upper quadrants of the FAST
Ultrasoundpodcast: Advanced Trauma podcast
FAST eller eFAST på traumarummet – vad är vinsten?
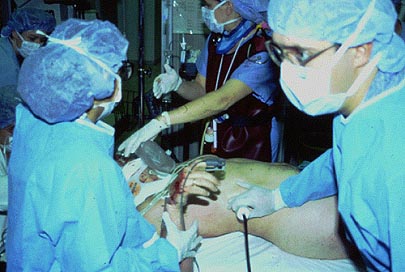
Sedan FAST-undersökningens tillkomst i traumabedömningen på 1970-talet i Tyskland och 1990-talet i resten av världen har mycket ändrats. Traumavården har centraliserats till truamacenter och de har i sin tur sett till att CT:n har lagts i nära anslutning. Tomografi-tekniken har dessutom utvecklats med snabbare körningar, tätare snitt mindre stråldos och bättre upplösning.
För traumamottagandet har det inneburit att de flesta patienter som har stora eller multipla traumatiska skador (major trauma) nu undersöks med en trauma-CT, dvs skalle, halsrygg, thorax, buk, bäcken, kotpelare. En meta-analys av 11 observationella studier (jiang-l-et-al-2016) visar att patienterna lämnar akuten/traumarummet snabbare om man gör trauma-CT jämfört med om man gör flera selektiva undersökningar. Det kanske inte är så konstigt. Däremot bör man fundera på det faktum att det inte var någon skillnad i vårdtid eller mortalitet mellan grupperna!
Men vad har FAST (eller extended FAST) för plats på traumarummet nu när CT:n är så tillgänglig, snabb och bra?
- Diagnostik av tillstånd som inte tolererar någon delay: Ventilpneumothorax och tamponad, massiv blödning i buken med behov av att omedelbart klampa aorta.
- Diagnostik av tillstånd där CT:n har låg sensitivitet: Kardiogen shock (inkl tamponad)
- Prognostisering av traumatiskt hjärtstopp: Finns det hjärtaktivitet?
Att ultraljud förbättrar diagnostik av pneumothorax vid trauma är väl belagt (blaivas-et-al-2005, ianiello-et-al-2014). Ultraljud har varit sättet att diagnostisera tamponad sedan slutet av 1960-talet (pridie-turnbull-1968) och har aldrig ifrågasatts. Om patienten är i svår shock och man med FAST kan konstatera att det finns en blödning i buken och inte finns någon tamponad kan det finnas en tidsvinst i att gå direkt på laparotomi och högt upp i buken klämma av aorta, jämfört med att göra en nödthoracotomi för samma ändamål, eftersom man i nästa andetag kan åtgärda blödningen.
I FAST och eFAST görs ingen annan kvalitativ bedömning av hjärtat än om det finns hjärtrörelser och om det finns perikardvätska. Om traumapatienten är i shock men det fortfarande finns någon minut tillgodo, kan ett fokuserat ultraljud av hjärtat tillföra mycket. Optimera genom att byta till en sektorprob (och cardiac mode). Då kan man också svara på följande; är patienten i shock pga hypovolemi? Är patienten i shock pga neurogen stunning/takutsubo? Är patienten i shock pga hjärtkontusion ( regional hypokinesi, oftast RA, RV)? Är patienten i shock pga traumatisk klaffskada (waterhammer effect – aortaklaffen, intrakardiell tryckökning – mitralisklaffen)?
Transthorakalt echo (TTE) har dock relativt låg sensitivitet för att upptäcka kontusion och klaffskada, TEE är bättre. Eastern Association for the Surgery of Trauma (EAST) har skrivit guidelines för trubbigt våld mot hjärtat: screening-for-blunt-cardiac-injury
Man kan diskutera om man alltid ska ta sig tid att göra en FAST, även när det finns indikation för nödthoracotomi; i en studie av inaba-et-al-2015 var NPV 100 % för att prediktera död genom att titta efter frånvaro av myokardrörelser vid FAST. Scancrit har skrivit ett bra inlägg om den studien och om FAST vid nödthoracotomi generellt: FAST thoracotomy
Bedömning av trauma med TEE?
För flera år sedan hade jag en traumapatient som hade fallit från hög höjd och hade ådragit sig flera extremitetsfrakturer, revbensfrakturer och hade GCS 3. Hen hade palpabla pulsar, intuberades på skadeplatsen utan läkemedel. Vid ankomst kunde vi känna femoralispulsar men när NIBP togs var trycket 55/30. eFAST (som utfördes parallellt) visade inget blod i pericardiet, ingen ptx, liten hemothorax vä, inget blod i buken. Slät-rtg bäcken u.a. Kliniskt ingen femur-fx. Efter några minuter var vi på op-salen (vägg-i-vägg med traumarummet på Karolinska) och kirurgen utförde en lateral thorakotomi och klämde av aorta descendens. Blodtrycket steg momentant till >100 varpå det utfördes en laparotomi som bekräftade att det inte fanns blod i buken. I vä thorax fanns ca 100 ml blod. På prov släpptes aorta – trycket föll. Manuella hjärtkompressioner gjordes – trycket steg. Berodde hypotensionen på en neurogen stunning av myokardiet?? Ett TEE visade en väldigt trött vänsterkammare med lite bevarad kontraktilitet basalt. Cirkulationen stabiliserades med adrenalin och noradrenalin-inf och lite senare med milrinon-inf. CT hjärna visade uttalade coup-contrecoup kontusioner.

I den här retrospektiva studien från Seattle gick man igenom echo-fynd hos 139 patienter med isolerad skallskada. Echo hade beställts på klinisk indikation (risk för selection bias). Patienter med känd hjärtsjukdom exkluderades. Av 139 hade 16 LVEF<50% och 21 regional dys/hypokinesi i vänsterkammaren;
Preliminary Report on Cardiac Dysfunction after Isolated Traumatic Brain Injury
Neurogen hjärtsvikt efter TBI?
Att aneurysmal subarachnoidalblödning (SAH) kan orsaka plötslig hjärtdöd, neurogen hjärtsvikt, neurogent lungödem, arytmier är ingen nyhet. Vid neurogen hjärtsvikt eller stunning (Neurogenic Stunned Myocardium – NSM) beskrivs vänsterkammaren echokardiografiskt som en japansk bläckfiskfångare, Tako-tsubo, med apikal och midventrikulär akinesi/hypokinesi. Den ledande hypotesen till tillståndets uppkomst är en massiv frisättning av katekolaminer sekundärt till en enorm ICP-stegring, som kräver enorm ökning av perfusionstrycket. I hjärtat frisätts noradrenalin direkt från sympatiska nervändar subendokardiellt och i en sån här cirkulatorisk katastrofsituation leder det till en urspårad metabolism och mitokondriedysfunktion i myocyterna. Histologiskt ses specifika förändringar som följer den sympatiska innerveringen snarare än kärlförsörjningen.
Mindre känt är kanske att en liknande (samma?) form av hjärtåkomma kan inträda efter TBI med eller utan traumatisk SAH. Flera mekanismer kan bidra till uppkomsten. En omedelbar stor blödning orsakar såklart en ICP-stegring. Vid alla former av svår TBI förekommer en kortare eller längre period med apné som leder till varierande grader av hyperkapni (se tidigare inlägg). Hyperkapnin leder till en momentan ICP-stegring som måste övervinnas med högre perfusionstryck, vilket ger motsvarande katekolaminfrisättning som vid en aneurysmal SAH.
Läs mer om NSM här: Cardiovascular complications of brain injury
Ultraljud av lungorna i primary survey?
Är det möjligt att överge slätrötgen av lungorna vid primary survey vid trauma? Om patienten är stabil och ändå ska undersökas med trauma-DT är svaret ja. Om patienten är instabil är läget annorlunda. Ultraljud kan snabbt utesluta pneumothorax och signifikant hemothorax. Tubläge om patienten är intuberad? Ja, om lung sliding finns bilateralt så ventileras båda lungorna. En sak som vi ännu inte har löst är dokumentationen – om vi ska fatta fler beslut baserade på ultraljud måste undersökningarna sparas så att vi kan granska oss själva i efterhand. Avseende möjlighet till eftergranskning är röntgen fortfarande bättre än ultraljud.
Test Characteristics of Ultrasonography for the Detection of Pneumothorax






Senaste kommentarer